Composición
Cada 100 ml de suspension oral contienen:
Ibuprofeno 4,00 g, sacarosa 62,50 g, lecitina de soja 0,10 g, metil p-hidroxibenzoato sódico 0,16 g, propil p-hidroxibenzoato sódico 0,02 g, ácido cítrico anhidro 0,56 g, citrato trisódico 0,50 g, esencia de frutilla 0,07 g, esencia de cereza 0,08 g, taumatina 0,00095 g, rojo allura 0,002 g, goma xántica 0,40 g, glicerol 10,00 g y agua purificada c.s.p. 100ml
Acción Terapéutica
Analgésico, Antiinflamatorio y antipirético
Indicaciones
Actron Pediátrico 4% contiene como ingrediente activo ibuprofeno, que es un analgésico (calma el dolor), antiinflamatorio (reduce la inflamación) y antipirético (baja la fiebre).
Se indica su uso para dolores reumáticos o musculares, de espalda, neuralgia, dolores de cabeza, dentales, menstruales y fiebre. Este producto alivia dolores, reduce la inflamación y la temperatura, además alivia los dolores asociados a estados gripales y resfrío común.
Caracteristícas farmacológicas / propiedades
Acción Farmacológica:
Grupo farmacoterapéutico: sistema musco-esquelético, fármaco anti-inflamatorio y anti-reumático, no esteroide, derivados del ácido propiónico.
Código ATC: M01AE01
Farmacodinámica:
El ibuprofeno es un derivado del ácido propiónico y pertenece al grupo de los analgésicos – antiinflamatorios no esteroides (AINEs). El fundamento de su actividad reside en la inhibición de la ciclo-oxigenasa y consecuentemente en la inhibición de la síntesis de prostaglandinas, ejerciendo sus propiedades analgésicas, antipiréticas y antiinflamatorias. Además, el ibuprofeno inhibe reversiblemente la agregación plaquetaria.
Farmacocinética:
El ibuprofeno administrado vía oral es rápidamente absorbido y distribuido en todo el cuerpo. Una vez metabolizado por el hígado (90% hidroxilado y carboxilado) sus metabolitos inactivos son completamente eliminados principalmente por los riñones, pero también por la bilis. La vida media de eliminación es aproximadamente 2 horas.
Datos preclínicos de seguridad:
Toxicidad aguda: los estudios para la toxicidad aguda en animales no han mostrado una sensibilidad inusual.
Toxicidad crónica: la toxicidad crónica y sub-crónica del ibuprofeno se ha manifestado en varias especies de animales, en especial en la forma de lesiones y úlceras del tracto gastrointestinal. La acción ulcerogénica se desarrolló primero a dosis de 300 mg/kg en ratones y 180 mg/kg en ratas, pero en dosis tan bajas como 8 mg/kg en perros.
Potencial mutagénico y tumorogénico: investigaciones in-vitro e in-vivo en bacterias y linfocitos humanos, no han mostrado evidencia de la acción mutagénica del ibuprofeno. Los estudios de carcinogenicidad en ratas y ratones no han dado ninguna prueba de la acción cancerígena del ibuprofeno.
Toxicidad reproductiva: estudios experimentales en dos especies de animales han demostrado que el ibuprofeno atraviesa la barrera de la placenta, pero no hay evidencia de efectos teratogénicos.
Posología/dosificación – modo de administración
Niños:
Para bajar la fiebre: a) si la temperatura es menor a 39°C (axilar), se recomienda administrar una dosis de 0,125 ml por cada kg de peso corporal (equivalente a 5 mg de ibuprofeno/kg/dosis) cada 6 a 8 horas, no más de 3 veces por día. b) si la temperatura es igual o mayor a 39°C (axilar), se recomienda administrar una dosis de 0,25 ml por cada kg de peso corporal (equivalente a 10 mg de ibuprofeno/kg/dosis) cada 6 a 8 horas, no más de 3 veces por día
Recordar que cada mililitro de suspensión de ACTRON Pediátrico 4% suspensión oral contiene 40 mg de ibuprofeno.
| Peso | Temp. menor a 39ºC | Temp. igual o mayor a 39ºC | Espacio entre dosis |
|---|---|---|---|
| Niños de 20 kg a 29 kg | 2,5 ml | 5 ml | 6 a 8 hs |
| Niños de 30 kg a 40 kg | 4 ml | 7,5 ml | 6 a 8 hs |
Dolores leves a moderados, dolor en las articulaciones y artritis reumatoidea: a) 20 a 40 mg/kg/día, dividido cada 6 a 8 horas (0,12 ml/kg a 0,25 ml/kg cada 6 a 8 horas), no más de 3 veces por día.
b) en pacientes con artritis reumatoidea juvenil con dolores leves se recomienda emplear una dosis de 20 mg/kg/día. Dosis máximas recomendadas: 40 mg/kg/día.
En niños menores de 6 años y/o de menos de 20 Kg de peso, es necesario ajustar la dosis de Actron Pediatrico 4%. Consulte con su pediatra de cabecera.
Adultos:
- Para el alivio de dolores y bajar la fiebre: 10 ml (400 mg) cada 6 u 8 horas.
- Dolores menstruales: 10 ml (400 mg) cada 4 horas.
- Artritis reumatoidea e inflamación de las articulaciones 1200 – 3200 mg/día dividido en tres a cuatro tomas.
Adultos mayores: No es necesario modificar las dosis.
Debería usar la menor dosis efectiva por el tiempo más corto que sea necesariopara aliviar los síntomas. Si usted tiene una infección, consulte a un médico sin demora si los síntomas (como fiebre y dolor) persisten o empeoran.
Modo de administración:
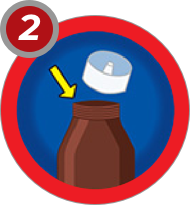
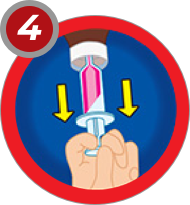
Los envases contienen una jeringa oral graduada de 5 ml. La jeringa se introduce en el tapón perforado, se invierte el frasco, se tira del émbolo hasta que el líquido alcance la marca en ml. o el equivalente al peso del niño, se vuelve el frasco a su posición inicial y se retira la jeringa.
La jeringa deberá limpiarse y secarse después de cada uso.
Puede administrarse el medicamento con las comidas.
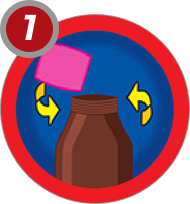
IMPORTANTE: DEBE AGITARSE EL FRASCO ANTES DE SU USO.
Contraindicaciones
No tome Actron Pediátrico 4%
- Si es alérgico a la aspirina, al ibuprofeno, a otro antiinflamatorio o a algún excipiente del producto.
- Si alguna vez presentó enfermedades alérgicas, (broncoespasmo, rinitis aguda, pólipos nasales, picazón) luego de tomar aspirina u otro medicamento para reducir la inflamación. Si está cursando el último trimestre de embarazo.
- Si bien el ibuprofeno está contraindicado en el 3° trimestre de embarazo, si usted está embarazada o planeando quedar embarazada consulte a su médico antes de tomar el medicamento debido a que no es recomendable su uso durante el mismo, puesto que podría afectar adversamente el embarazo y/o al desarrollo embriofetal. Sumado al riesgo aumentado de abortos espontáneos.
- Tiene o ha tenido úlcera o hemorragia en el estómago.
- Tiene o ha tenido sangrado gastrointestinal o perforación debido al uso de medicamentos para reducir la inflamación.
- Enfermedades inflamatorias intestinales.
- Padece de enfermedad del hígado, riñones o corazón.
- No use este producto en niños menores de 6 meses.
ADVERTENCIAS Y PRECAUCIONES
Tenga especial cuidado con Actron Pediátrico 4%
- No debe ser usado para dolores abdominales.
- Se deberá consultar con el médico si está tomando aspirina.
- Si está tomando otros medicamentos para reducir la inflamación.
- El riesgo de presentar un efecto secundario puede disminuir tomando la menor dosis durante el menor tiempo posible.
- Si es mayor de 65 años.
- Si tiene antecedentes de enfermedades inflamatorias gastrointestinales, de hipertensión arterial y/o falla cardiaca. Si tiene disfunción hepática, antecedentes de disfunción renal.
- Tiene problemas de estómago (ardor estomacal, acidez).
- Si usted consume tres (3) o más vasos diarios de bebida alcohólica.
- Suspenda su uso y consulte con su médico si experimenta alergias y reacciones serias en la piel, como erupción en la piel y picazón, que puede acompañarse de dificultad para respirar, hinchazón de labios, lengua, garganta o cara.
- Suspenda su uso si experimenta empeoramiento de asma.
- Si presenta toxicidad gastrointestinal, sangrado o ulceración, deberá suspender el tratamiento y consultar con su médico.
- Hable con su médico o farmacéutico si usted tiene una infección (ver “Infecciones”).
Interacción del ibuprofeno con otros medicamentos y con alimentos:
Informe a su médico si está utilizando o ha usado recientemente otros medicamentos, incluidos los adquiridos sin receta. El consumo de alcohol puede aumentar el riesgo del daño a la mucosa gastrointestinal y el sangrado. No usar en combinación con aspirina (ácido acetilsalicílico).
Fertilidad, embarazo y lactancia:
- Fertilidad: Hay poca probabilidad que este producto pueda incidir sobre la fertilidad femenina afectando la ovulación. Este efecto es reversible con la suspensión del tratamiento.
- Embarazo: no se recomienda el uso de ibuprofeno durante el embarazo. El tratamiento puede afectar al embarazo y/o al desarrollo embriofetal. No tomar ibuprofeno durante el primer y segundo trimestre de embarazo cuando no sea estrictamente necesario, manteniendo una dosis baja, durante el menor tiempo posible. No se debe tomar ibuprofeno en el tercer trimestre de embarazo.
- Lactancia: el ibuprofeno puede pasar en pequeñas cantidades a leche materna, pero el riesgo de afectar al bebé parece improbable a las dosis indicadas. Si el tratamiento fuera prolongado o si se toman cantidades mayores deberá considerar interrumpir el amamantamiento.
Infecciones:
- Actron Pediátrico 4% puede esconder los signos de infecciones como la fiebre y el dolor. Por lo tanto, es posible que Actron Pediátrico 4% pueda retrasar el tratamiento para la infección, lo que puede llevar a un aumento del riesgo de complicaciones. Esto se ha observado en neumonía causada por bacterias e infecciones bacterianas de la piel relacionadas a la varicela. Si usted toma este medicamento mientras sufre una infección y los síntomas infecciosos persisten o empeoran, consulte a su médico sin demora.
Posibles efectos secundarios:
- Poco común: dolor abdominal, náuseas, trastornos en el sistema digestivo (dispepsia); urticaria, picazón, sarpullido; dolor de cabeza.
- Raro: diarrea, flatulencia, constipación y vómitos.
- Si ocurre esto o experimenta cualquier otra reacción, consulte a su médico y suspenda su uso.
Sobredosis
Si toma más Actron Pediátrico 4% del que debiera:
En Argentina: Ante la eventualidad de una sobredosificación, concurrir al hospital más cercano o comunicarse con los centros de toxicología:
- Hospital de Pediatría Ricardo Gutiérrez: Tel. (011) 4962-6666/2247.
- Hospital A. Posadas: Tel. (011) 4654-6648/4658-7777.
- Centro de Asistencia Toxicológica La Plata: Tel. (0221) 451-5555
Presentación
Cada 100 ml de suspensión oral contienen: Ibuprofeno 4,00 g, Excipientes: sacarosa, lecitina de soja, metil p-hidroxibenzoato sódico, propil p-hidroxibenzoato sódico, ácido cítrico anhidro, citrato trisódico, esencia de frutilla, esencia de cereza, taumatina, rojo allura, goma xántica, glicerol y agua purificada c.s.p.
En Argentina: Envases con 30, 100 ml o 180 ml con jeringa dosificadora.
Mantener fuera del alcance de los niños.
Conservar a temperatura ambiente inferior a 25°C. No almacenar en heladera.
Ante cualquier inconveniente con el producto el paciente puede llenar la ficha que está en la Página Web de la ANMAT: http://www.anmat.gov.ar/farmacovigilancia/Notificar.asp o llamar a ANMAT responde 0800-333-1234
® Marca registrada de Bayer AG, Alemania.
Kaiser-Wilhem-Allee 1, 51373, Leverkusen - Alemania
Fabricado según fórmula original y bajo licencia de Bayer AG, Alemania en Coronel Méndez N°438/440, Wilde, Pcia. de Buenos Aires, para BAYER S.A., Ricardo Gutiérrez 3652, (B1605EHD), Munro, Buenos Aires.
Director Técnico: José Luis Role, Farmacéutico.
Especialidad Medicinal autorizada por el Ministerio de Salud.
Certificado N° 43910 CCDS 03
Representa y distribuye Bayer S.A., Av. Santa Teresa Nº 2245 casi Av. Aviadores del Chaco, Asunción - Paraguay. Telef.: 617 3500. D.T.: Verónica Patricia Acosta Ubaldi - Reg. Prof. 1869. Venta autorizada por D.N.V.S. del M.S.P. y B.S. Registro sanitario N° 10852-03-EF.
En caso de sobredosis, acudir al Centro Nacional de Toxicología - Emergencias Médicas. Teléf.: 204-800.
Importado y Distribuido por Bayer Boliviana Ltda., Av. Las Ramblas Edificio Tacural II Piso 2, Centro Empresarial (Equipetrol Norte) Santa Cruz, Bolivia. R.S. No. II-61120/2017. D.T.: Lic. Susana Antezana Ameller.
Condición de venta: Venta libre.
Este medicamento por contener glicerol como excipiente puede ser perjudicial a dosis elevada, puede provocar dolor de cabeza, molestias de estómago y diarrea.
Este medicamento contiene 3,125g de sacarosa en 5ml, lo que deberá ser tenido en cuenta en pacientes con intolerancia hereditaria a la fructosa, problemas de absorción de glucosa/galactosa, deficiencia de sacarosa/isomaltasa y pacientes diabéticos.